

2026-04-17
行业资讯
前 情 提 要
在ADC系列文章的上一篇《双载荷ADC篇》中我们讨论到单载荷 ADC 逼近治疗窗极限后,双载荷试图以多机制协同突破耐药与异质性瓶颈,但协同不会自动发生,毒性叠加、配比失衡、系统复杂度剧增反而会压缩安全窗口。当载荷与分子设计已被反复讨论,ADC 的体内暴露与剂量逻辑又藏着哪些关键约束?为什么 ADC 无法像普通药物一样 “按需加量”?
【PharmaLegacy ADC系列·第六篇】
在所有ADC相关讨论中,剂量问题几乎是最容易被误解的环节之一。与小分子药物不同,ADC的给药剂量通常偏低,调整空间也十分有限。即便疗效尚未完全释放,剂量往往也会先受到安全性约束,而难以像传统化疗或单抗那样继续上调。
这种现象并非源于开发策略保守,而是ADC药代动力学特性与系统行为共同作用的结果。对ADC而言,剂量从来不是一个单纯决定暴露强度的参数,它同时牵动分布路径、清除机制、组织摄取和毒性触发位置。也正因为如此,ADC的剂量设计并不遵循“给得更多、进瘤更多、疗效更强”的线性逻辑,而更接近于在多重系统约束下寻找一个可维持的暴露平衡。
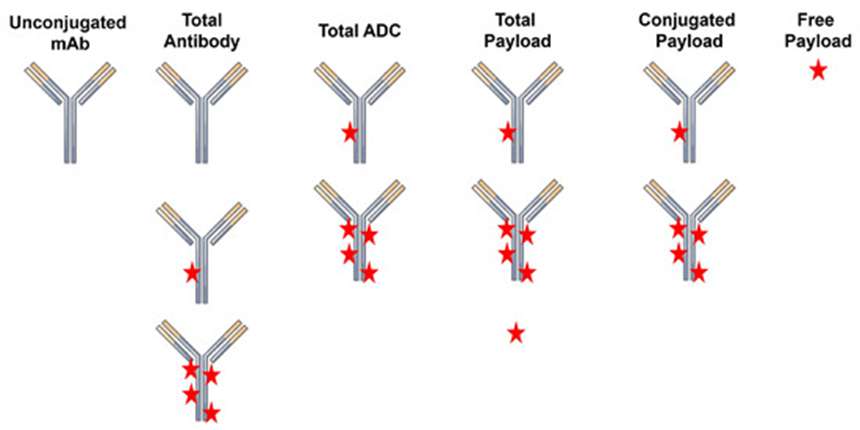
DOI: 10.3390/cancers18010005
1、ADC剂量设计的理想假设
在理想状态下,剂量逻辑似乎应当相当直接:给药剂量越高,系统暴露越大,进入肿瘤的有效payload数量也越多,疗效随之增强;当毒性出现时,再通过剂量回退寻找治疗窗口。
这一逻辑在小分子药物中通常成立,在裸抗中也往往可以部分适用。但当payload被偶联到抗体上之后,这一假设却不一定成立。ADC的剂量不只影响暴露水平,也会同步改变分子的体内运行方式。随着剂量上调,被放大的除了潜在抗肿瘤效应,同样包括非靶组织摄取、降解处理以及游离payload释放所带来的系统暴露。换言之,ADC的剂量问题不是拉到多高的剂量更有效,而是增加的暴露将首先流向哪里。
2、现实运行方式:ADC的PK更像抗体×毒素的乘积
在体内,ADC的PK并不是一条单一曲线,而是多个层级叠加后的综合表现。完整ADC的循环时间主要由抗体决定,因此其分布与清除在相当程度上接近裸抗;payload的系统暴露则取决于ADC在何处被摄取、何时被降解,以及payload是否具备组织扩散能力;当游离payload产生后,其后续代谢又可能呈现出与传统小分子完全不同的特征。
更关键的是,这三个层级并不是彼此独立的。给药剂量一旦上调,完整ADC暴露增加,非靶组织中的摄取也同步上升,继而推动payload在非靶位置释放和累积。于是,ADC的剂量提升并不意味着更多药物进入肿瘤,反而可能更早遇到耐受性问题。对ADC而言,PK特性是一个由抗体递送、组织处理和payload暴露共同构成的复合系统。
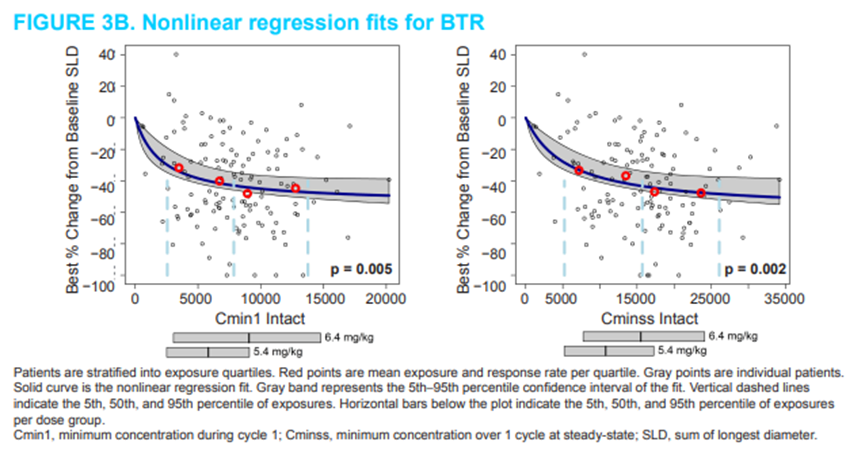
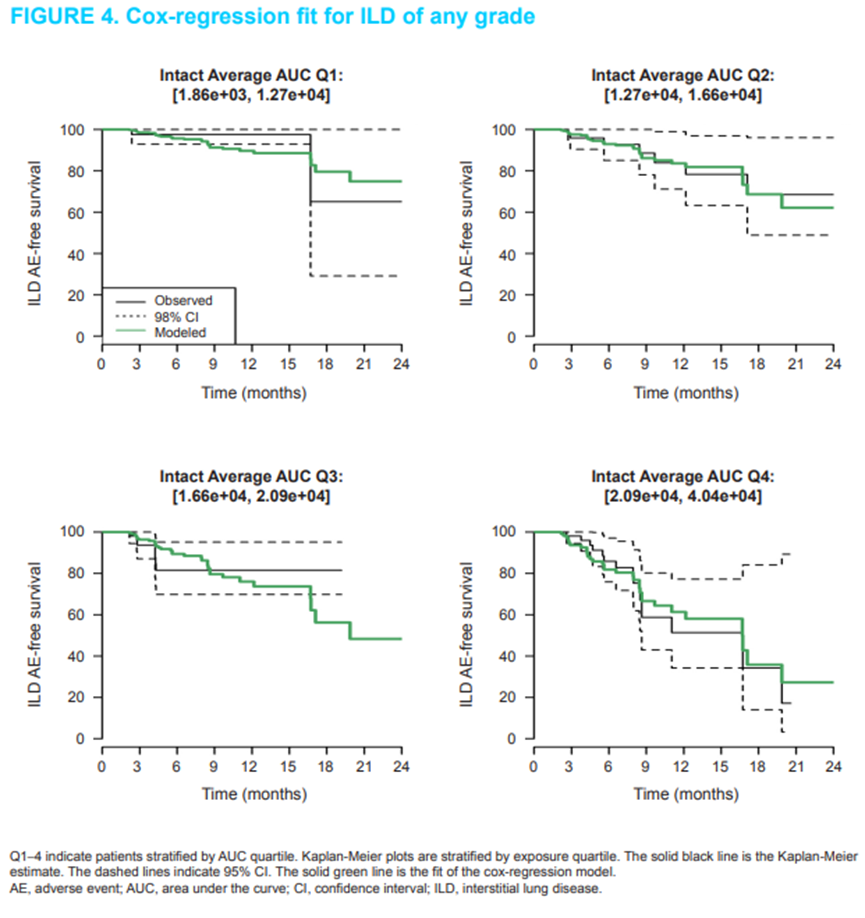
Presented by Daiichi Sankyo, on ASCPT 2019 Annual Meeting
3、由此带来的结构性代价:暴露—疗效关系提前转折
在多数ADC项目中,暴露—疗效曲线不会持续平滑上升,常常在较早阶段就进入平台区。超过某一剂量后,肿瘤内payload增量有限,毒性风险却开始明显增加。
其背后的逻辑并不复杂。肿瘤组织的可及性本身受限,抗体在实体瘤中的渗透和分布并不能无限提高;相反,非靶组织对ADC的摄取并不存在同样意义上的饱和,甚至还可能因为抗原池而放大。因此,当剂量继续上调时,系统暴露首先被放大的往往不是肿瘤通路,而是非靶通路。结果就是,ADC的最大可耐受剂量(MTD)很多时候并不由肿瘤需求决定,而更接近于由正常组织的承载能力所决定。也正是在这一点上,ADC与传统细胞毒药物或裸抗拉开了很大差异:剂量越高,并不必然意味着疗效越好。
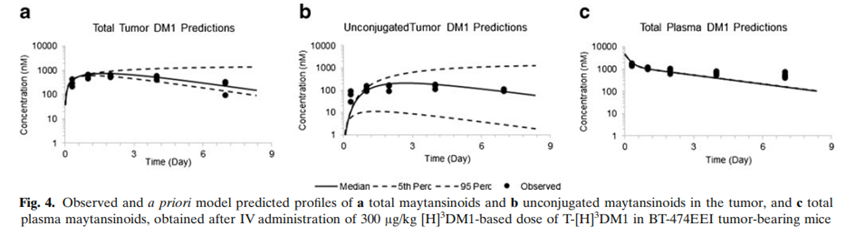
DOI:10.1208/s12248-016-9904-3
4、NHP PK与临床剂量转化:更适合用于识别风险而非直接换算剂量
在ADC研发中,非人灵长类动物(NHP)长期被用于剂量与安全性评估,但实践已经反复表明,NHP中观察到的耐受剂量并不能简单外推为临床安全剂量。
原因在于,ADC毒性通常由payload相关的系统暴露驱动,而这一路径在不同物种间并不完全一致。即便抗体交叉反应良好,Fc介导摄取、组织分布、内吞处理、FcRn相关回收以及代谢降解过程,仍可能存在显著差异。这些差异足以改变同一ADC在不同物种中的暴露格局与毒性器官分布。因而,NHP数据在ADC剂量设计中的真正价值,更多在于帮助识别风险器官、毒性模式和潜在剂量边界,而不是直接提供一个可线性换算的临床起始剂量。对ADC而言,跨物种转化更像是在比较系统行为,而不是在换算剂量。
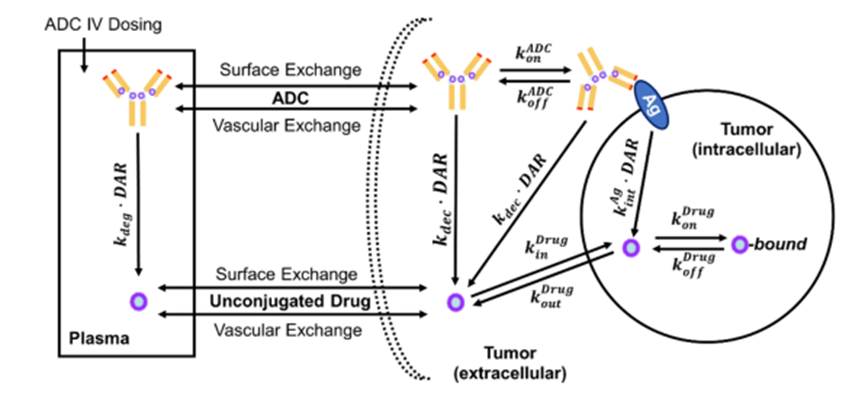
DOI:10.1007/s10928-025-09978-3
示意图总结了ADC在血液与组织间分布、内皮细胞吞饮进入内体后与 FcRn 结合介导回收/转运、未结合进入溶酶体降解,以及降解/脱偶联导致 payload 释放并形成系统暴露的关键路径。由于FcRn相关过程、组织摄取与降解/脱偶联等参数在不同物种间存在差异,同一ADC在NHP中观察到的耐受性更适合用于识别风险器官与毒性模式,而非直接推导临床安全剂量。
5、给药策略:剂量管理而非剂量追求
这也解释了为什么,ADC临床开发中的关键往往不是持续加量,而是优化给药策略。分次给药、阶梯递增(step-up dosing)、延长给药间隔,本质上都不是为了突破剂量上限,而是在既定耐受边界内重新分配暴露时间,使payload效应在毒性全面暴露之前尽可能释放。
在这一框架下,一些ADC即便采用相对较低的名义剂量,仍然能够取得显著疗效;而继续上调剂量时,所增加的系统负担往往快于疗效增益。剂量管理因此成为ADC临床设计中的核心能力之一。除了更高的单次给药量,价值也可能体现在有限的剂量能否被更有效地转化为可持续的肿瘤暴露和可管理的安全性。
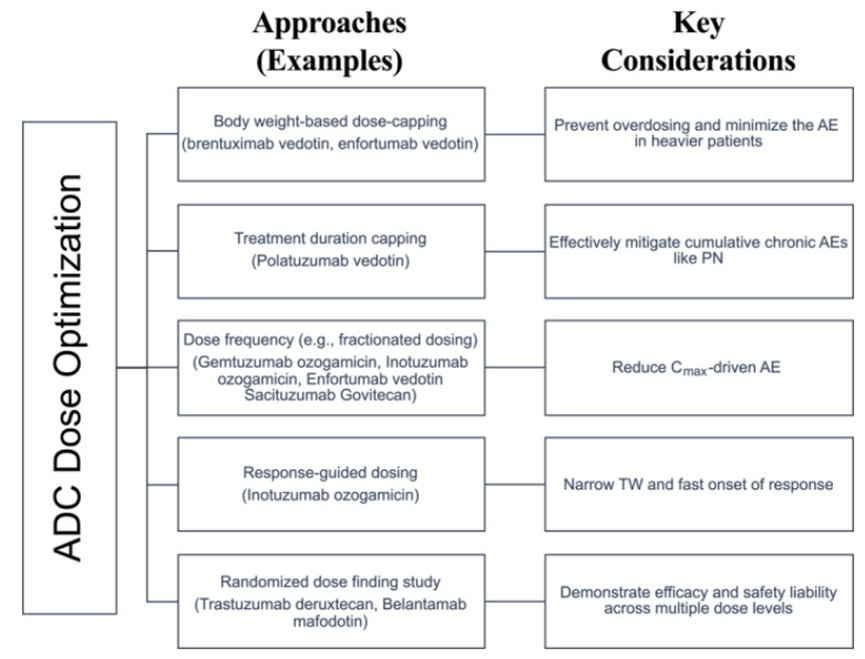
DOI: 10.1002/cpt.2278
6、从研发与转化角度看,PK阶段最关键的判断
在ADC项目中,除了还能不能继续剂量爬坡,还有几个更基础的判断可能影响决策:肿瘤内payload暴露是否仍会随剂量上调而增加,非靶组织暴露路径是否已经开始主导系统行为,以及当前观察到的毒性是否与同类payload的已知经验相互印证。
如果这些问题的答案逐渐转向负面,继续提高剂量往往只会更快推动分子触发系统毒性,而难以带来等比例的疗效回报。此时,限制因素未必来自给药策略本身,也可能更早就在payload性质、linker稳定性、组织分布逻辑中决定。对研发与转化团队而言,PK阶段的关键任务除了为分子争取“更高剂量”,也需要尽早判断这个分子的系统边界究竟由什么决定,以及这一边界是否有通过各种手段重新优化利用的空间。
7、结语|ADC的剂量,是系统边界的体现
ADC的剂量决定,并不是一个带有靶向能力的小分子药物式的简单加法问题,而是一系列系统性约束的外在体现。它综合反映了抗体分布、payload毒性、linker稳定性以及生物体承载能力的共同边界。
因此,对ADC开发而言,关键并不在于一味提高剂量,而在于更有效地利用有限剂量,并准确识别暴露在何处开始偏离肿瘤通路、毒性又在何处率先成为限制因素。只有完成这一判断,PK才真正能够转化为可操作的开发策略。这也是ADC区别于传统药物开发的重要特征之一。
本系列最后一篇将聚焦ADC 毒理学核心:从 NHP 到临床,哪些毒性信号真正值得警惕?如何读懂毒理数据并判断临床转化风险?作为收官篇,我们将完整闭环 ADC 从设计到临床的全系统逻辑。
敬请期待:
【PharmaLegacy 专业ADC系列·第七篇】毒理篇:从NHP到临床,哪些信号真正值得警惕