

2026-04-24
行业资讯
前 情 提 要
在ADC系列文章的前六篇中,我们依次拆解了抗体决定 ADC 递送边界、双抗 ADC 的复杂度平衡、Linker 主导释放可控性、Payload 定义疗效与毒性、双载荷的协同与风险、PK与剂量的体内约束逻辑,完整走完了ADC从分子设计到体内行为的全链条。当设计、载荷、递送、剂量都已逐一解析,ADC 迈入临床前最后一关:毒理信号如何解读?从 NHP 到临床,哪些风险真正决定项目生死?本期为PharmaLegacy ADC 系列收官终篇,我们将从毒理视角闭环全系统逻辑,告诉你哪些信号值得警惕、如何判断临床转化可行性,为整个系列画上完整句号。
【PharmaLegacy ADC系列·第七篇】
在ADC的研发路径中,毒理学常被视为进入临床前的最后一道关卡。当一个项目完成药效、PK与CMC验证后,毒理研究似乎承担着一项明确而具体的任务:确认最大耐受剂量(MTD),识别潜在靶器官,并为首次人体给药提供安全依据。
但在项目推进中,ADC的毒理研究不止是一个合规步骤。它往往是系统性问题最早集中暴露的阶段,也是连接工程假设与临床现实的关键节点。对ADC而言,毒理学并不只是回答安不安全,它更深层地回答的是,这个分子在真实生物体系中,将以什么方式首先失控。
1、ADC毒理的理想定位:识别可转化风险
在理想状态下,ADC的毒理研究应当完成三项任务:识别主要剂量限制性毒性(DLT),判断毒性与靶点、生物分布或payload机制之间的关联,并为临床起始剂量和剂量递增策略提供依据。
这一逻辑在传统小分子药物中相对成立,但在ADC体系中很难得到如此直接的答案。ADC毒性通常并非由单一机制驱动,而是抗体分布、payload系统暴露与组织特异易感性共同作用的结果。正因如此,ADC毒理结果很少只是一个简单的“安全”或“不安全”判断,更常见的情形,是它提供了一组需要按照正确方式解读的信号。对研发团队而言,这些数据的价值除了在哪个剂量下看到毒性,还有这些毒性出现的方式、节奏与归因是否能够支持后续转化判断。
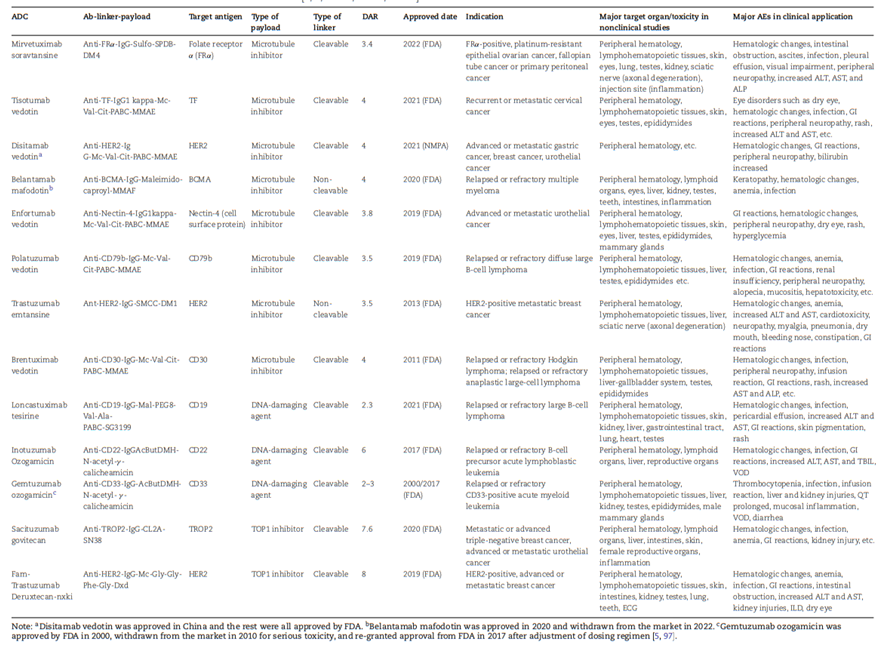
DOI: 10.1016/j.pharmthera.2019.04.008
2、NHP 毒理并不等同于“安全背书”
非人灵长类动物(NHP)之所以被广泛用于ADC毒理研究,主要在于其Fc受体体系、组织分布以及部分靶点表达更接近人类。但大量实践已经反复提示,NHP的耐受性并不能被直接等同为临床安全性。
这种不对称性在ADC领域并不罕见。一方面,某些on-target/off-tumor毒性在NHP中并不显著,但会在临床中持续出现;另一方面,一些在NHP中观察到的毒性,在临床中又未必成为真正的限制因素。其根本原因在于,ADC毒性高度依赖payload的系统暴露、组织敏感性以及分布路径,而这些因素在不同物种之间很难完全重合。也因此,毒理的价值更多在于揭示毒性是如何形成的,而不是简单回答这个分子是不是有毒性。对ADC而言,跨物种毒理判断的重点除了表面耐受剂量,更多是系统行为是否呈现出具有转化意义的模式。
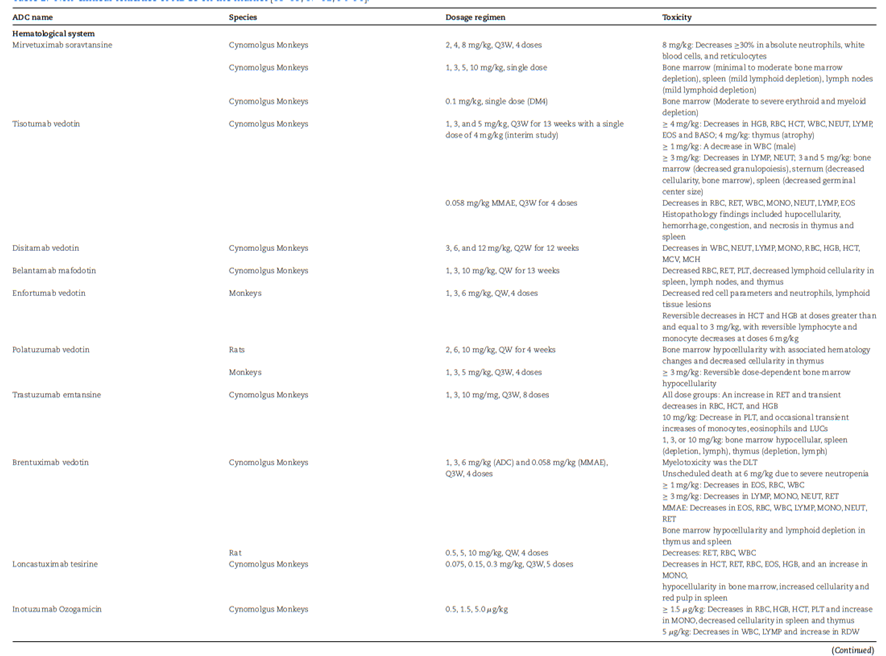
DOI: 10.1016/j.pharmthera.2019.04.008
3、毒性类型的可预测性:payload驱动而非靶点驱动
如同前文所述,已上市ADC及大量临床项目中,可以观察到一个高度一致的规律:毒性类型在很大程度上由payload机制塑造,而非主要由靶点决定。
微管抑制剂类payload常伴随外周神经毒性和骨髓抑制;maytansinoid类payload与血小板减少和肝毒性高度相关;拓扑异构酶I抑制剂类payload则常与胃肠道毒性和间质性肺病风险联系在一起。这些毒性在不同靶点、不同抗体背景下反复出现,呈现出鲜明的机制特征。对研发判断而言,这一规律的重要性非常直接:当观察到的毒性模式与payload既往经验高度一致时,其在临床中复现的概率往往更高;而一旦毒性表现明显偏离既有经验,就不能只把它视为噪音,而需要进一步警惕是否存在新的分布路径、释放路径或组织摄取机制。
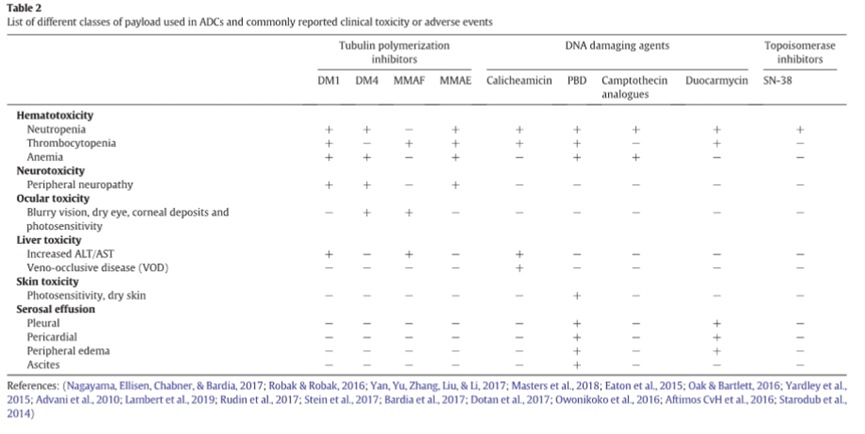
DOI: 10.1093/abt/tbaf004
4、剂量与毒性的关系:最早出现的毒性往往最关键
在ADC毒理评估中,一个常见误区是把注意力过度集中在最高剂量组的毒性表现上。但是那些最早出现、并且随着剂量递增迅速加重的毒性反而可能有更大的临床意义。
原因并不复杂。ADC的剂量上限通常由系统暴露最敏感的组织决定。一旦某一组织在较低剂量下即出现不可逆或难以管理的损伤,这类信号在临床中往往会率先成为限制因素。相比之下,一些仅在极高剂量下出现、且具有明确可逆性的毒性,未必会对临床剂量设计形成真正约束。
5、NHP → 临床的相关性:哪些信号值得高度重视
在实际转化过程中,最值得高度警惕的,通常是那些与payload已知机制高度一致、同时又呈现出明确剂量依赖性的毒性。这类信号在临床中往往具有较高复现概率,也意味着其管理策略需要在试验设计阶段提前纳入考量。
同样需要重视的,是发生在非靶组织中、并与抗体分布或Fc介导摄取相关的毒性。此类信号往往提示payload的主要暴露路径并不局限于肿瘤内释放,而是沿系统性摄取扩展。另一个经常在早期被低估、却在临床中迅速放大的风险,是重复给药后逐步累积、且恢复不完全的毒性。这类信号之所以重要,并不只是因为它们提示“有毒”,而是因为它们更接近真实临床长期给药条件下的情况:一旦毒性呈现累积性和恢复不全,其在多周期治疗中往往更快转化为实际限制因素。
6、从研发与转化角度看,毒理阶段最关键的判断
在ADC项目中,毒理研究真正需要回答的问题并不是在某个剂量下有没有毒性,而是毒性是否可预测、可管理,以及是否存在规避空间。
如果毒性来源与payload机制高度一致,且缺乏通过给药策略或工程优化进行缓解的可能,那么项目继续推进的风险就需要慎重考虑。相反,若毒性表现与分布路径或剂量节奏高度相关,往往仍可能通过工程设计或给药方案调整争取一定空间。当某些毒性信号在不同工程变体和策略尝试下反复出现时,通常提示其背后存在更为结构性的来源,而不是某个单一因素所致。对ADC研发而言,这一判断的重要性并不亚于药效结论本身,因为它可能决定项目是否会在临床阶段被迫终止。
7、结语|ADC 的毒理,是系统理解能力的试金石
在ADC体系中,毒理学并不是研发流程的终点,而是对前期所有假设的一次系统性检验。它检验抗体选择是否合理,检验linker与payload是否匹配,也检验研发团队是否真正理解这个分子在体内的运行方式。
当毒理信号被正确解读时,它提供的并不只是警告,也包括明确的优化方向。
至此,这一系列从抗体、linker、payload、PK到毒理的讨论,构成了一个相对完整的逻辑闭环:作为一个复杂的系统工程,ADC的成功,并不取决于某一个模块做到极致,而取决于研发团队是否能够理解并优化系统边界。毒理之所以重要,也正因为它最集中地暴露了这种系统理解能力是否真正成立。