

2026-04-07
行业资讯
前 情 提 要
在ADC系列文章的前三篇中,我们逐步论证了ADC是一个高度耦合的系统:抗体篇指出抗体决定了分布边界与安全窗口;双抗ADC篇探讨了双靶向在突破单表位局限的同时也引入了系统复杂度陷阱;Linker篇揭示了连接子与偶联技术的核心在于可控性而非理想化设计。进入第四篇,我们将聚焦Payload:更高的payload毒性是否必然带来更宽的治疗窗口?旁观者效应在改善肿瘤异质性覆盖的同时,是否也在同步放大正常组织的暴露风险?为什么说payload的选择,本质上是在研发早期接受一类特定的毒性模式?
【PharmaLegacy ADC系列·第四篇】
在ADC的三大核心构件中,payload往往是最容易被直观理解、也最容易被过度放大的变量。它决定肿瘤细胞在完成ADC内吞后将承受多强的细胞毒打击,也常常主导一个项目在体外实验中呈现出的药效强度。
也正因如此,ADC早期关于payload的设计逻辑,长期围绕更高毒性展开。在抗体递送效率有限、肿瘤异质性普遍存在、靶点表达并不均一的现实条件下,提高单分子层面的杀伤能力,似乎是一条直接的补偿路径。但随着ADC从概念验证走向真实临床开发,这一路径的边界也越来越清楚:payload抬高的并不只是药效上限,它同样在持续定义ADC的安全边界,并且往往率先决定治疗窗的宽窄。
10.3390/ph17101338
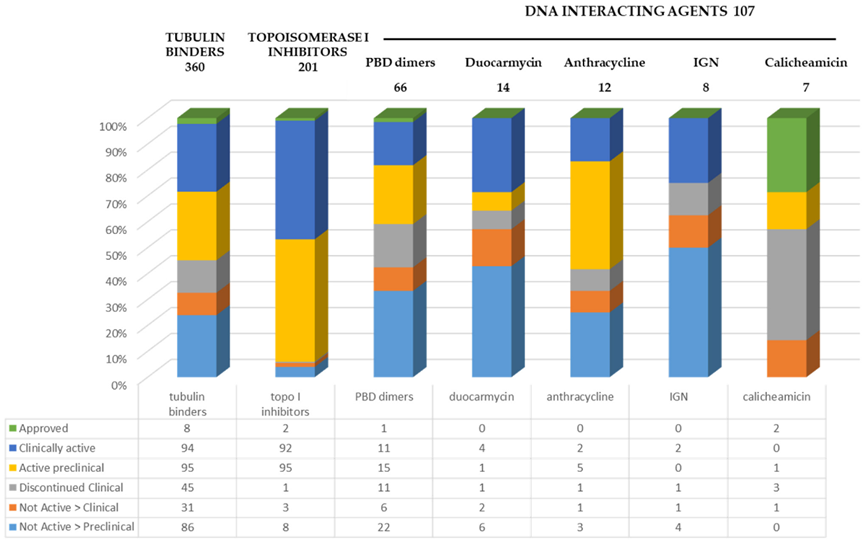
在研ADC的payload类型分布
相关统计显示,产业重心正从微管抑制逐步向 Topo I抑制剂和DNA互作类机制扩展,部分原因在于这类机制在处理肿瘤异质性和旁观者效应方面展现出潜在优势;与此同时,它们也引入了新的系统毒性挑战。
1、Payload在ADC设计中的理想角色
在理想化模型中,payload的角色相对明确:它需要具备极高的细胞毒性,使有限数量的药物分子在进入肿瘤细胞后仍足以触发不可逆的细胞死亡;同时,其分子特征还必须适合偶联与递送,以便沿抗体介导的内吞路径被有效带入靶细胞。
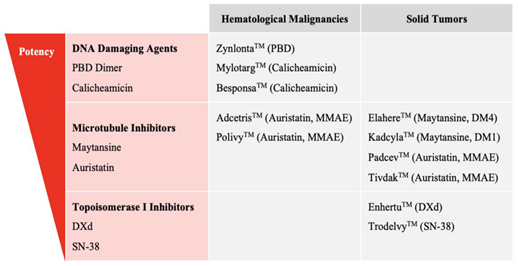
沿着这一逻辑回看,ADC的发展历程几乎可以视为payload不断演进的过程:从早期的calicheamicin、maytansinoids,到auristatins,再到拓扑异构酶I抑制剂以及更近一步的DNA损伤相关机制,payload的效力持续提高,适用范围也随之扩展。
但一旦进入真实体内环境,payload面对的就不再只是肿瘤细胞内的局部杀伤。设计层面的靶向递送虽然能够提高暴露选择性,却不足以将payload的作用严格限制在靶细胞内部。对ADC而言,payload因此从来不是一个孤立的药效模块,而是一个会同时牵动分布、释放、代谢与耐受性的系统变量。
2、现实运行方式:Payload的暴露远不止发生在靶细胞内
在体内,payload的真实暴露远比理想假设复杂。即便在linker稳定、抗体选择合理的前提下,payload仍可能通过非特异性内吞、Fc介导摄取、linker缓慢水解以及ADC在正常组织中的代谢降解进入非靶组织。
这些暴露事件在单次给药中未必十分突出,但在多周期给药条件下会逐步累积,并最终转化为可观测的毒性谱。大量临床数据表明,即便靶向完全不同的抗原,使用相同或相似payload的ADC,仍常呈现高度相似的剂量限制性毒性(DLT)模式。这个现象说明,在系统层面,抗体更多决定送达何处,而payload更深刻地决定到达后会造成何种后果。
3、由此带来的代价:治疗窗口的系统性收缩
这也解释了ADC开发中一个反复出现的问题:payload毒性的提升,并不会线性转化为更宽的治疗窗口。相反,在不少项目中,更高强度的payload更早表现为毒性剂量前移。
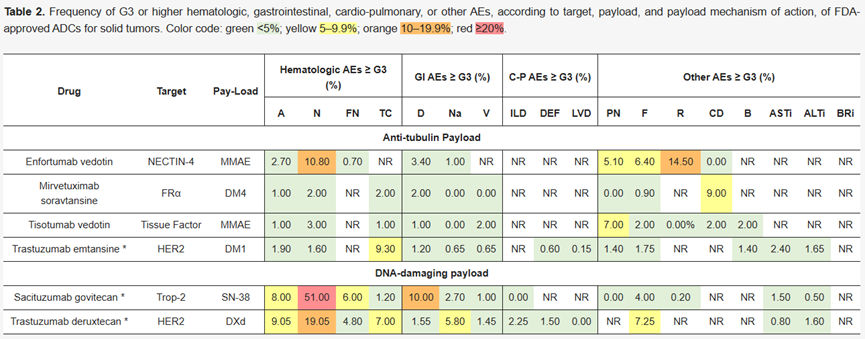
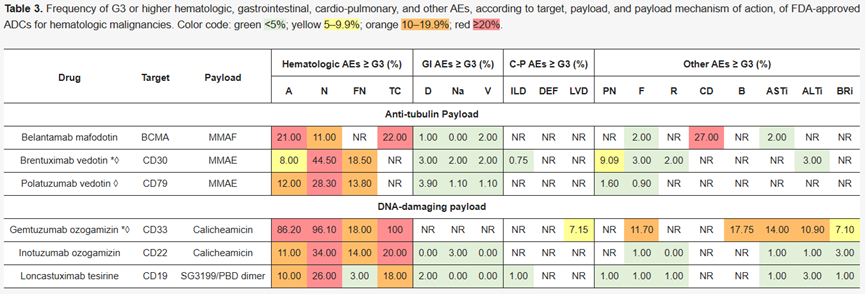
以微管抑制剂类payload为例,外周神经病变和骨髓抑制在多个采用MMAE或MMAF的ADC中反复出现;maytansinoid类payload则长期与血小板减少和肝毒性相关;而拓扑异构酶I抑制剂类payload虽然在实体瘤中显示出更强的疗效潜力,也同时带来了间质性肺病、胃肠道毒性等新的安全性挑战。类似现象在不同项目间高度复现,说明这些毒性更接近payload作用机制在系统暴露背景下的延伸结果,而非偶发事件。
因此,很多时候真正限制剂量上探的,并非靶点本身或抗体结合能力,而是payload在非理想分布条件下暴露出的机制性毒性。这也是为什么一个在细胞水平上表现极强的payload,并不必然对应一个在临床上更可用的分子。
10.3390/pharmaceutics17020258
4、旁观者效应:疗效突破与毒性扩散的同一枚硬币
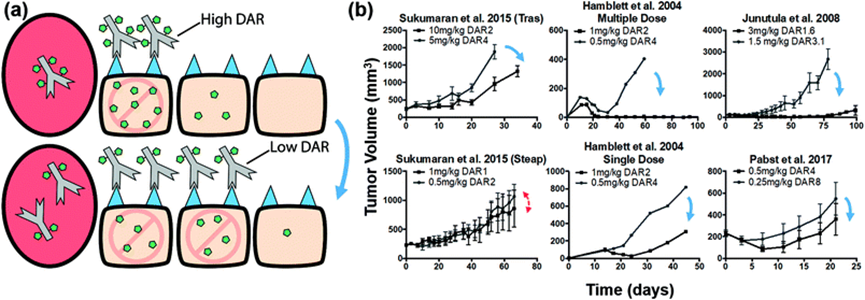
旁观者效应通常被视为应对肿瘤异质性和低抗原表达的重要机制。当payload具备膜通透性后,即便未直接内吞ADC的肿瘤细胞,也可能因邻近细胞释放的毒素而受到杀伤。在HER2-low等场景中,这一机制已被成功利用,并成为Enhertu取得疗效突破的重要基础之一。
但从系统视角看,旁观者效应并不只发生在肿瘤内部。只要payload能够在组织间扩散,其作用范围就很难天然局限于肿瘤局部,相应的毒性影响范围也会被同步放大。换言之,旁观者效应并不是一个单向增益项,而是一种需要被精细调校的系统属性。它能否真正转化为净临床获益,高度依赖于抗体分布特性、组织暴露格局、给药策略以及患者个体差异。
10.1039/C7ME00093F
5、Payload的选择,本质上是对毒性模式的选择
如果从临床结果反推,payload的选择在很大程度上就是在开发早期接受一类特定的毒性模式。虽然疗效差异会受到靶点生物学、内吞效率、肿瘤负荷和患者分层等多重因素影响,但毒性类型往往更稳定地由payload本身塑造。抗体、靶点和适应症改变了有效递送效率和获益人群,却很少从根本上改写payload在系统层面的生物学代价。
因此,payload的核心价值不单在于更新或更强,更在于其毒性是否能够被提前识别、是否具有相对清晰的剂量依赖关系、是否能够通过给药策略、监测策略和患者筛选部分管理,以及这种毒性轮廓是否与适应症的疾病特征和临床获益空间相匹配。
这也意味着,项目在payload选择阶段就需要完成一次反向临床思考:研发团队应尽早判断,这一payload最可能在哪类器官、哪类患者、哪类给药节律下暴露出边界;又有哪些风险能够通过PK建模、生物标志物监测和临床管理策略部分对冲。只有把这些问题前移,payload筛选才真正具备开发决策意义。
MAbs. 2023 Jan-Dec;15(1):2229101.
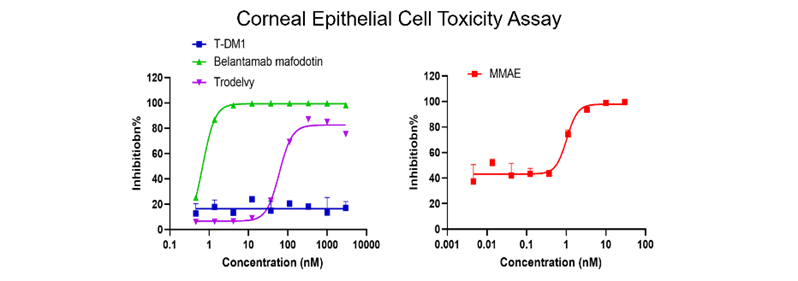
6、结语:Payload决定疗效上限,也决定安全性的边界
在ADC体系中,payload并非简单的杀伤工具。它一方面帮助ADC突破抗原密度、内吞效率和肿瘤异质性带来的限制,另一方面也通过系统暴露、组织扩散和机制性毒性持续压缩治疗窗。
如果说过去一代ADC payload竞争的核心在于能否做出药效,那么下一阶段更关键的问题,可能在于谁能更稳健地控制疗效与安全性的平衡。进一步说,下一代payload竞争所考验的,未必只是活性高低,更在于其是否能够作为一个真正的工程化可预测系统组件融入开发体系。
ADC系列文章第五篇,我们将讨论双载荷ADC。这一策略尝试将两种不同机制的payload整合于同一抗体分子,以期克服耐药和肿瘤异质性,但同时也显著提高了系统复杂度,可能使治疗窗口被更早压缩。目前产业界对此仍持谨慎推进态度,这是否说明双载荷ADC的难度被低估了?
敬请期待:
【PharmaLegacy 专业ADC系列·第五篇】双载荷ADC篇:从单机制杀伤走向多机制协同的下一代ADC技术