

2026-03-16
行业资讯
前 情 提 要
在ADC系列文章的上一篇中我们讨论到,当单抗ADC的识别维度成为瓶颈时,双抗可作为重构系统的新路径,但其成败取决于早期的系统评估。识别决定药物“去哪儿”,而Linker与偶联技术则决定药物“何时释放、如何释放”。当“稳定性设计”进入真实体内环境与CMC体系,它将面临哪些非预期挑战?
【PharmaLegacy ADC系列·第三篇】
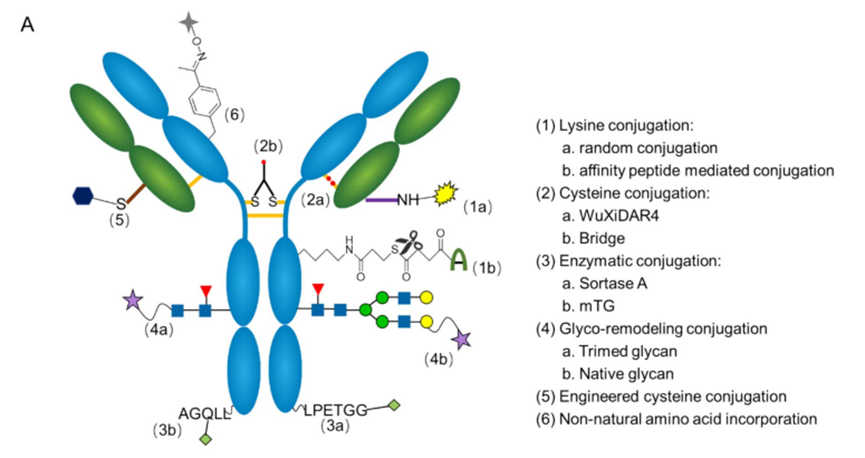
在抗体偶联药物(ADC)的三大核心构成要素——抗体、payload与linker中,linker与conjugation技术通常被归类为偏工程化的模块。从最初的设计逻辑来看,它们承担着两个相对明确的任务:在系统循环中保持结构稳定,避免payload提前释放;同时在ADC进入靶细胞后,又能够在细胞内环境中被有效切断,使payload得以释放并发挥细胞毒作用。
在这一工程框架下,linker往往被视为一个可以通过化学结构持续优化的技术变量。当某一ADC分子在体内表现不理想时,研发团队通常首先考虑是否可以通过更换linker类型、调整切割机制或优化偶联位点来改善系统稳定性与释放效率。
然而,在真实的ADC研发与转化过程中,linker的作用远不止于一个简单的“连接组件”。大量项目经验表明,linker本身很少是单独导致项目失败的原因,但却常常成为最早暴露系统不匹配问题的模块。许多ADC项目在推进过程中遇到困难,并不是因为linker设计不够先进,而是因为这一设计被嵌入了一个已经接近系统极限的分子体系之中,从而放大了原本就存在的分布与暴露问题。从系统角度看,linker更像是ADC整体体内行为的一个放大器,而不是一个可以被孤立优化的结构变量。
10.1093/abt/tbaf010
1.理想设计框架:稳定性与释放效率之间的工程平衡
在分子工程层面,linker设计本质上是一种稳定性与可释放性之间的平衡。ADC在血液循环中需要保持足够稳定,以避免payload在到达靶组织之前发生脱落,从而降低系统毒性;与此同时,一旦ADC通过抗原介导内吞进入肿瘤细胞,linker又需要能够在溶酶体环境中被有效切割,使payload能够迅速释放并发挥杀伤作用。
基于这一逻辑,目前ADC领域形成了两种主要设计策略。一类是可切割linker,其释放依赖细胞内特定生物环境,例如蛋白酶活性、酸性条件或还原环境;另一类则是不可切割linker,这类设计依赖抗体在细胞内的完全降解,从而释放出payload-linker残基。
不同ADC产品对这一平衡的选择体现了不同的设计哲学。例如 Kadcyla 采用不可切割 SMCC linker,其payload在细胞内释放后仍带有残余结构,从而限制其跨膜扩散能力,这种设计显著降低了旁观者效应,同时也在一定程度上控制了系统毒性。相比之下,Adcetris 以及 Enhertu 等药物采用可切割linker,通过在肿瘤细胞内快速释放payload,并允许其在组织中一定程度扩散,从而在抗原表达存在异质性的肿瘤中获得更强的杀伤效果。
从工程角度看,这些设计并不存在简单的优劣之分,而是在不同生物学条件下对稳定性与释放效率所做出的权衡。
2.linker稳定性并不是一个独立变量
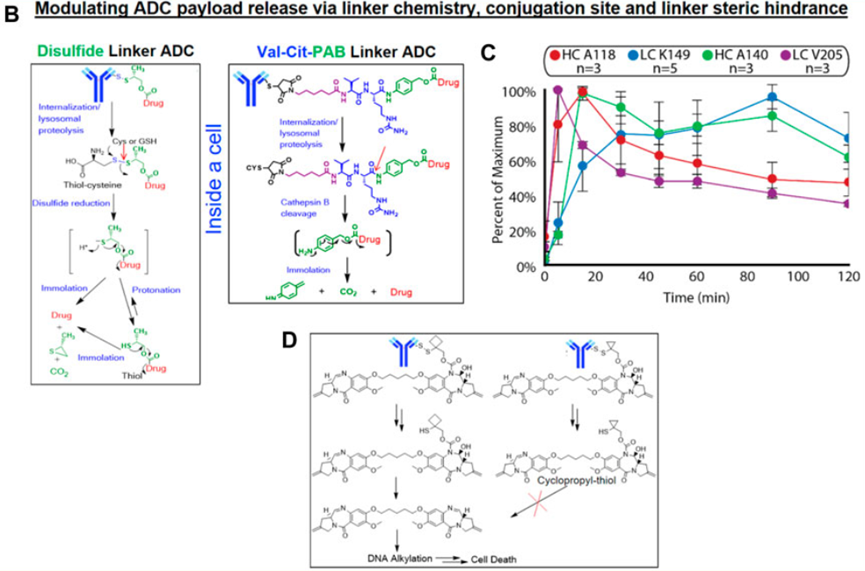
10.3389/fphar.2021.687926
在真实体内系统中,linker的行为始终与ADC整体动力学紧密耦合。抗体在体内的组织分布、抗原介导内吞速率以及payload本身的理化性质,都会对最终的释放行为产生显著影响。因此,单独讨论linker稳定性往往无法解释ADC在体内的真实表现。
在许多ADC项目中,真正决定payload体内暴露水平的关键因素并不是linker是否稳定,而是ADC分子在体内被哪些组织摄取。如果ADC在循环过程中被单核吞噬系统或其他非靶组织大量吞噬,即使linker在血浆环境中表现出高度稳定性,payload仍然会在这些组织的溶酶体中释放,从而对正常组织造成损伤。
从系统动力学角度来看,linker稳定性能够控制payload释放的时间,但却无法决定释放发生的组织位置。也正因为如此,在部分ADC项目中,即使linker稳定性得到明显改善,PK曲线中完整ADC的暴露水平有所提高,临床毒性表现却未必随之明显改善。这一现象在多个ADC开发项目中都曾被观察到。
3.linker设计改变的是毒性的空间分布
当linker设计被放回整个ADC系统框架中进行评估时,一个重要现象逐渐显现:linker稳定性的提升并不会线性扩大药物的治疗窗口。在抗体分布已经决定非靶组织摄取占主导的情况下,更稳定的linker往往只会延迟payload释放,而无法改变释放发生的组织位置。
与此同时,linker类型还会显著影响payload在组织中的扩散行为。可切割linker通常能够产生所谓的“旁观者效应”,即释放的payload可以扩散至邻近肿瘤细胞,从而扩大杀伤范围。这一机制在抗原表达高度异质的肿瘤中尤为重要,也被认为是 Enhertu 等新一代ADC能够在部分实体瘤中取得较好疗效的重要原因之一。然而,这种扩散能力同时也会增加payload在正常组织中的暴露风险,从而带来更复杂的毒性谱。
相比之下,不可切割linker释放的payload-linker残基通常具有较低的膜通透性,因此更多局限于被ADC内吞的细胞内部发挥作用。这种设计降低了payload在组织中的扩散能力,但也限制了其对抗原表达不均一肿瘤的杀伤范围。
因此,从系统层面来看,linker并不是一个单纯用于降低毒性的工具,而更像是一个调节毒性空间分布的工程参数。
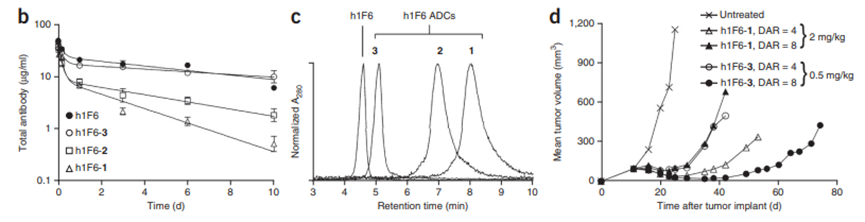
10.1038/nbt.3212
4.偶联技术真正解决的问题:分子异质性
在ADC工程设计中,另一个关键挑战来自DAR分布所带来的分子异质性。在传统随机偶联体系中,ADC分子通常形成DAR 0–8不等的混合群体,其中高DAR亚群往往具有更高疏水性,更容易被单核吞噬系统识别并清除,同时也更容易发生非特异性组织摄取。
这种异质性在体内往往会被放大,其影响远大于体外分析所呈现的结果。因此,近年来发展起来的位点特异性偶联技术,并不仅仅是为了获得一个更加“漂亮”的DAR数值,而是为了压缩DAR分布范围,从而减少分子层面的系统噪音。
通过限制DAR分布并提高结构均一性,这些工程化偶联策略能够显著提高ADC药代动力学行为的可预测性,并在CMC放大过程中提供更好的批次一致性。然而需要注意的是,这类技术并不会从根本上改变ADC在体内的分布逻辑,它们所提供的优势更多体现在工程可控性层面。
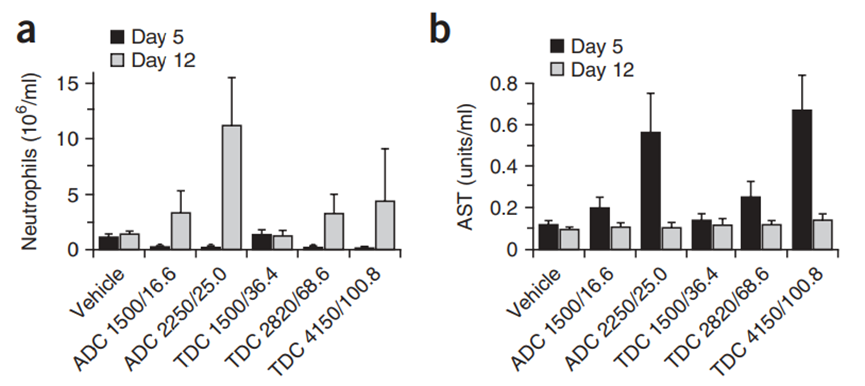
Doi: 10.1038/nbt.1480
5.行业趋势:从“最先进设计”转向“最可预测设计”
如果观察过去十余年已上市ADC的设计路径,可以看到一个明显趋势:行业逐渐从追求理论上最复杂、最先进的linker设计,转向更加可预测、可放大的工程方案。
这一变化并不意味着ADC技术创新的停滞,而是整个行业在系统复杂性与工程可控性之间做出的现实权衡。当ADC进入CMC放大与长期稳定性评估阶段时,linker与conjugation设计中的任何微小不确定性,都可能在工艺放大过程中被显著放大,最终表现为批次差异、产品质量波动甚至潜在的临床风险。
因此,在真实工业环境中,许多概念上极具吸引力的linker设计最终停留在临床前阶段,而那些经过反复验证、看似更加保守的方案却更容易进入临床并最终实现商业化。这一趋势也反映出ADC研发正在逐渐从单纯的分子设计问题,转变为一个更加典型的系统工程问题。
6.结语
linker并不决定ADC是否成立,但决定其工程可控性。在ADC系统中,linker更像是一个工程边界的调节器,而不是一个可以无限放大的技术杠杆。它无法弥补抗体选择不当或靶点生物学所带来的结构性问题,但却能够决定这些问题在系统中以何种形式暴露出来,从而影响项目整体的研发风险、毒性谱以及CMC可制造性。
在当前ADC技术阶段,对linker作用的理解已经逐渐从单纯的稳定性优化,转向对整个系统行为的调节。理解这一点,也许比设计一个更加复杂的linker结构更加重要。
在ADC系统中,linker与偶联技术决定了药物的释放节奏与可控边界。但当释放行为趋于稳定,真正决定治疗窗口上限的,便转向了另一个核心变量——payload的强效杀伤,究竟在多大程度上侵蚀着安全边界?
下一篇,我们将深入探讨:payload的选择为何本质上是对毒性模式的选择?以及,当“更强”的 payload 不断涌现,治疗窗口是被放大还是进一步压缩?
敬请期待:
【PharmaLegacy 专业ADC系列·第四篇】Payload 篇:当“强效杀伤”开始侵蚀治疗窗口