

2026-03-09
模型相关
目前,以dupilumab为代表的IL-4Rα抗体奠定了包括特应性皮炎和哮喘等2型炎症相关疾病的治疗基石:它通过阻断IL-4/IL-13信号,有效降低皮损与瘙痒,并在长期使用中形成相对稳定的安全与临床经验体系。与此同时,JAK抑制剂以其口服便利性和快速起效补足了另一端的需求,但也因其安全性问题在使用上受到一定程度的控制。
而在此背景下,Corvus Pharmaceuticals披露其首创口服ITK抑制剂Soquelitinib在特应性皮炎(AD)早期临床研究中的最新数据后,引发了业内较高关注。该研究显示出较为积极的药效信号:在第8周时EASI75 (湿疹面积和严重程度指数较治疗前基线水平改善≥75%)的应答率高达75%且耐受度良好,显示出具备与主流系统疗法对标的潜力。其之所以受到高度关注,除了药效和安全性优势外,同时证明了一条与IL-4Rα抗体不同的治疗逻辑,有望同时满足深度应答与疾病稳定性这两个重要临床价值,从而构成对IL-4Rα抗体市场地位的结构性挑战。
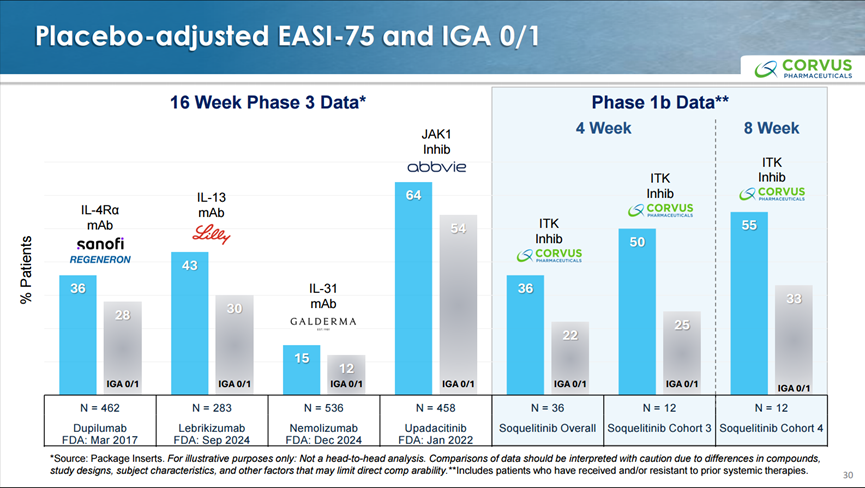
从阻断细胞因子到改变T细胞分化:ITK的定位决定了其竞争方式
IL-4Rα抗体的作用路径非常清晰:它在免疫细胞的效应端阻断IL-4/IL-13信号,抑制2型炎症的发生与放大。因此在以Th2轴为核心驱动的患者中表现稳定可靠。而ITK(IL-2 inducible T-cell kinase)对应的则是另一种思路。ITK位于T细胞受体(TCR)信号传导网络中,是影响T细胞激活阈值与分化走向的重要节点。临床上我们看到的Th2细胞因子谱(IL-4/IL-5/IL-13)是由T细胞在抗原刺激与共刺激环境中完成分化后分泌产生。而ITK抑制剂的理论优势在于它并非只拦截某一个下游因子,而是倾向于在更上游影响T细胞的分化程序本身,从根源上阻止或降低细胞因子的产生。
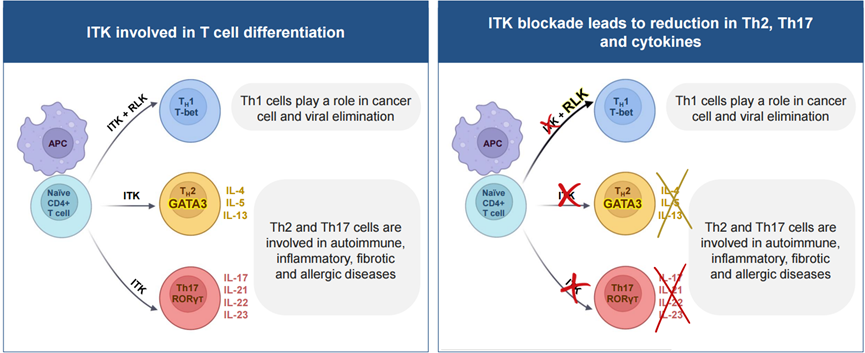
这也是为什么Corvus的材料中会强调Soquelitinib对Th2与部分Th17相关信号通路的影响,并将Treg水平的上升作为免疫重建与免疫平衡恢复的关键证据。从机制上看,当免疫系统由以促炎性Th细胞为主导的状态,转向以调节性T细胞占优势的免疫状态时,其意义不仅体现在临床症状的改善,更在于有望实现更低的复发风险,并在停药后仍可维持缓解状态。因此,相较于IL-4Rα抗体仅阻断单一效应通路,ITK抑制剂更接近于对T细胞炎症表型进行上游重塑的干预策略,这也为其在混合炎症表型疾病中的潜在优势提供了理论基础。
威胁IL-4Rα抗体,不只在初治,也在换药与升级
ITK抑制剂对IL-4Rα抗体的潜在影响,未必首先体现为在初治人群中的直接替代,更可能率先显现于临床实践中最常见、也最具挑战性的治疗场景,即部分应答与复发。
相较于病理异质性更高、表型更复杂的哮喘,AD在免疫分型清晰度与临床终点方面相对更易于早期验证。而在真实世界中,IL-4Rα抗体已暴露出相当规模的应答不足人群,表现为残余皮损持续存在、瘙痒控制不充分或复发频繁。对这部分患者而言,核心临床问题在于当以Th2轴为核心的治疗已无法实现充分疾病控制,下一步的治疗策略应如何选择。传统路径下,临床选择主要集中在两类方案:一是转向JAK抑制剂,二是在生物制剂框架内进行机制升级或联合用药。ITK抑制剂的机会窗口正出现在这一治疗决策节点上,其作用机制不同于单纯的Th2通路阻断,而是通过更上游的T细胞信号调控,理论上能够更好地覆盖那些并非由单一Th2轴驱动、而是伴随Th17信号参与或上游免疫驱动持续存在的复杂炎症表型患者。
因此,从竞争格局的角度看,ITK对IL-4Rα抗体的“威胁”并不局限于作为一线基准治疗的直接替代,更可能体现在对换药与机制升级市场增量的吸收。一旦后续研究能够在dupilumab部分应答或复发人群中建立稳定、可重复的临床证据,处方迁移与市场增量再分配将具备较高的发生概率。
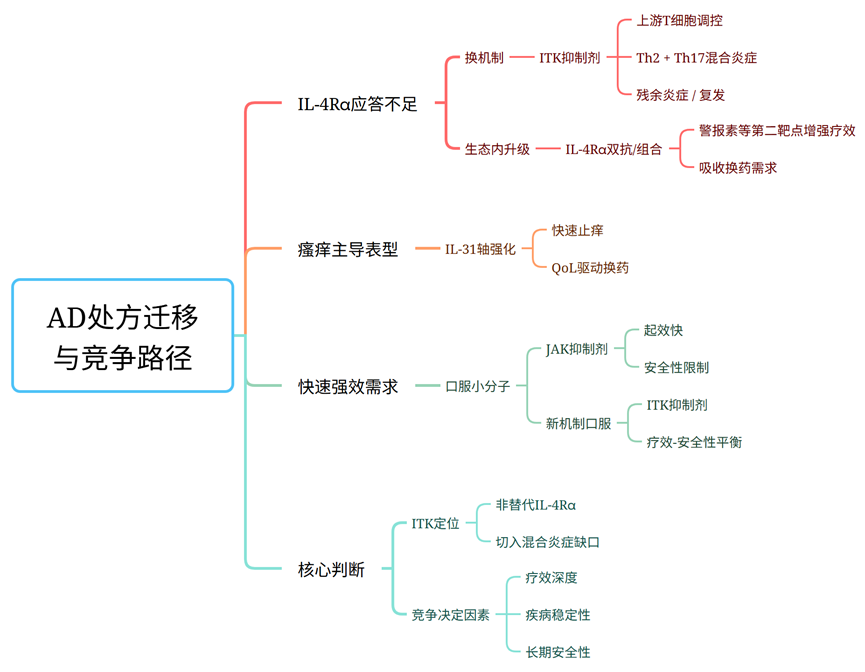
从机制到临床表型:ITK能否在的长期安全与维持上超越JAK
对口服小分子而言,要真正挑战生物制剂,其竞争的终极问题仍集中在两个硬指标上:长期安全性与维持策略。JAK抑制剂已经在临床上验证了口服小分子可以实现强效免疫抑制,但与此同时,其与感染风险、心血管事件乃至血栓相关的安全性信号,也使临床与监管机构普遍将其定位为需要严格风险管理、适用于特定人群的治疗选择。若ITK抑制剂希望进入更广泛人群并实现长期用药,其前提在于证明自身不会复制JAK抑制剂所面临的安全性困境。
这一差异的根源,恰恰体现在两类药物的作用机制上。JAK抑制剂通过干预多种细胞因子依赖的信号通路,对免疫及非免疫细胞均产生广谱影响,覆盖范围极广,因此在带来显著疗效的同时,也更容易牵动多条关键生理通路;相比之下,选择性ITK抑制剂目前显示出更为聚焦的作用特征,主要影响T细胞的活化与分化过程。若这种相对特异的免疫调控能够在临床上得以维持,并仅伴随可接受水平的感染风险,ITK 抑制剂有望形成一种区别于 JAK的口服免疫调节范式——兼具口服给药的便利性与接近生物制剂的长期使用潜力。从竞争格局的角度看,ITK若要构成对IL-4Rα抗体的长期威胁,必须同时跨越疗效与长期安全性这两道门槛。现有早期临床数据在疗效层面已提供初步支持,且尚未观察到显著的严重安全性信号,整体耐受性表现良好;但其能否在更大样本量及长期用药背景下持续维持可接受的风险–收益比,仍有赖于后续临床研究的系统性验证。
IL-4Rα的应对方向:通过双抗与联合策略,将“升级需求”留在既有生态内
当ITK以更上游的免疫调控能力和更广谱的通路覆盖展开竞争时,IL-4Rα阵营的最优策略,未必是试图在通路广度上正面硬碰硬,而更可能是通过双抗或联合治疗,精准解决临床中已暴露出的应答不足问题,从而削弱患者转向全新作用机制的动力。其核心目标在于:在既有治疗生态内完成疗效“升级”,而非将升级需求拱手让给新机制药物。
在特应性皮炎(AD)领域,至少存在两条具有明确策略价值的强化路径。第一类是引入更上游的“警报素”通路(如TSLP、IL-33/ST2等),以改善复发控制能力并覆盖更复杂的炎症表型;第二类则是围绕瘙痒这一高权重临床终点,通过加强IL-31等关键止痒通路,提升起效速度与症状缓解强度,从而整体增强疾病控制水平。上述策略的本质,并非构建新的治疗范式,而是在IL-4Rα已确立为AD基准治疗的前提下,充分利用其长期安全性数据与临床使用经验,通过机制补强来扩大患者覆盖范围,以对冲小分子免疫调节剂带来的竞争压力。
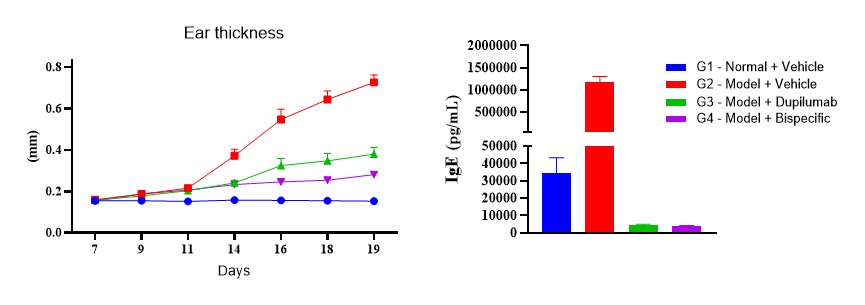
适应症外延:SSc等纤维化疾病决定ITK的“平台属性”上限
尽管当前ITK抑制剂的竞争焦点主要集中在AD领域,但从靶点属性与机制特征来看,其长期定位显然不应被局限为皮肤病新药。除AD外,哮喘同样与Th2炎症密切相关,但其免疫表型异质性显著更高。基于ITK对T细胞分化及炎症反应的上游调控特性,该机制在理论上更可能适用于IL-4Rα阻断疗效不佳、且呈现Th2与Th17信号并存的哮喘亚群,尽管这一假设仍有待前瞻性临床试验的验证。
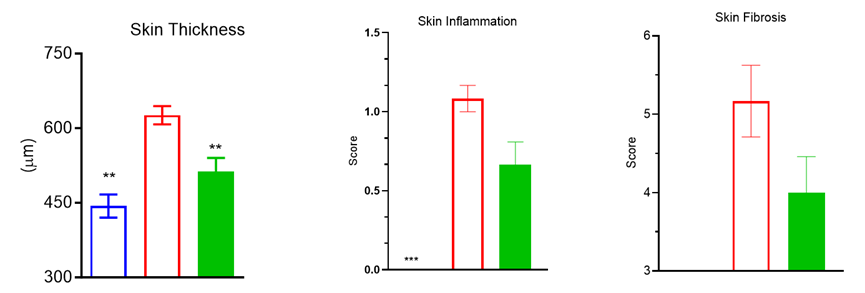
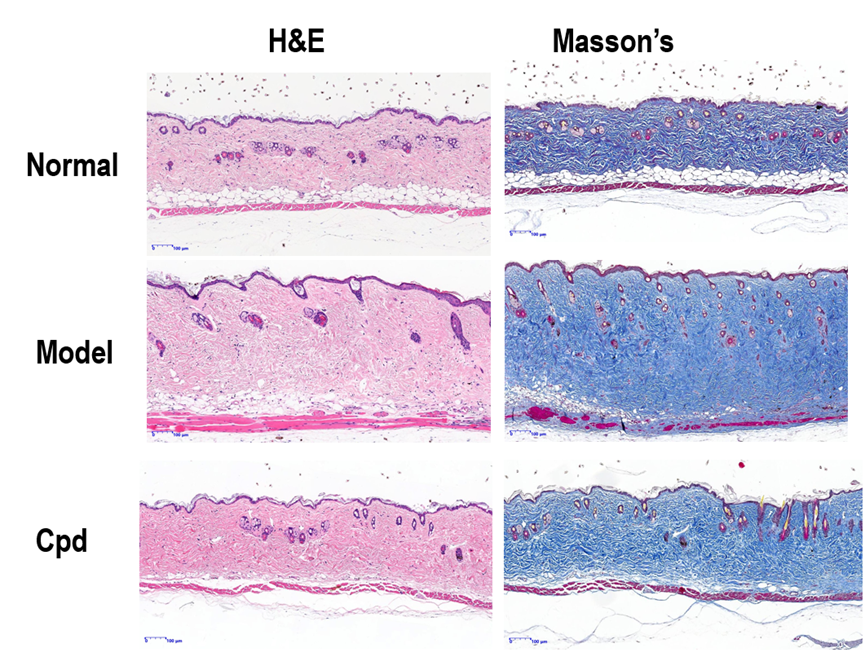
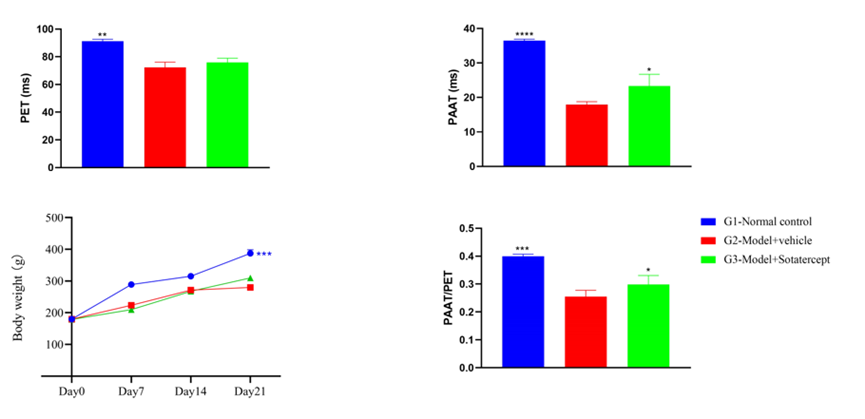
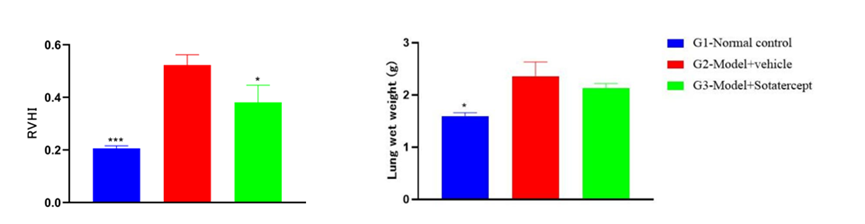
更为重要的是,已有临床前研究提示,ITK抑制剂在系统性硬化症(SSc)及其相关疾病,包括间质性肺纤维化、肺动脉高压等中也显示出积极效果。若这一信号能够在临床阶段得到确认,ITK的价值将不再局限于作为AD领域挑战IL-4Rα的口服升级方案,而是有望跃迁为覆盖多适应症的免疫调节平台型靶点。这一转变将显著重塑市场对ITK靶点价值边界的认知,也为同一通路上的其他候选药物打开新的战略入口,其竞争对象将不再是某一单一适应症中的基准治疗产品,而是在更广泛的疾病谱系中争夺上游免疫调节剂入口的位置。
Systemic Sclerosis
Pulmonary Arterial Hypertension
结语
总体而言,ITK 抑制剂的潜在价值,或许并不在于直接替代IL-4Rα抗体这一既有基准治疗,而在于凭借其更上游的免疫调控特征,针对IL-4Rα轴阻断应答不足、复发以及混合炎症表型等尚未被充分满足的临床缺口,提供一条差异化的治疗路径。Soquelitinib在特应性皮炎(AD)中公布的早期随机对照数据,为ITK抑制这一机制首次建立了与生物制剂进行同台比较与系统讨论的现实基础。在竞争路径上,ITK对IL-4Rα抗体治疗格局的影响,更可能并非源于初治人群的正面替代,而是从部分应答或复发患者中的处方迁移逐步展开,其核心竞争力将建立在明确的机制差异之上。未来这一竞争边界的最终形态,仍有赖于后续临床研究的验证:一方面,ITK抑制剂能否在维持疗效深度与疾病控制稳定性的同时,建立可支持长期用药的安全性特征与维持治疗策略;另一方面,IL-4Rα阵营是否能够通过双抗或联合方案,在上游驱动信号与瘙痒等关键临床维度实现生态内升级,从而有效吸收换药与机制升级需求。
在这一背景下,我们期待与对相关免疫机制及转化研究感兴趣的合作伙伴展开深入交流,共同推进围绕ITK通路和IL-4Rα为基础的联用及多抗的临床探索与验证。