

2026-04-07
模型相关
GLP-1多重激动剂的设计突破与代谢革命
1、为何走向“多靶点协同”?
尽管以GLP-1受体(GLP-1R)为靶点的单靶点激动剂在糖尿病和肥胖治疗中已确立里程碑式地位,但其疗效天花板和机制局限性日益显现:减重疗效易进入平台期;胃肠道不良反应影响部分患者的治疗耐受性;对胰岛素敏感性的改善及肝脏脂肪的清除作用有限。
为突破上述瓶颈,代谢疾病治疗的策略正从“单点精准打击”转向“多通路协同调控”。多重激动剂通过单一分子同时作用于多个与代谢密切相关的受体,旨在模拟并增强人体内源性激素网络的协同生理调节,实现“1+1>2”甚至“1+1+1>3”的系统性代谢改善。
2、靶点选择的科学逻辑:建立协同增效的代谢调控网络
2.1. GLP-1R:代谢调控的“核心枢纽”
GLP-1R的激活是疗效基石。它能促进葡萄糖依赖性胰岛素分泌、抑制胰高血糖素释放、延缓胃排空,并通过中枢神经系统增强饱腹感。然而,单一激活GLP-1R难以全面解决能量代谢失衡和胰岛素抵抗等核心病理问题。
2.2. GIPR:从“促肥嫌疑”到“协同伙伴”的科学认知转变
传统上,葡萄糖依赖性胰岛素释放多肽(GIP)因其潜在的促脂质储存作用而被谨慎看待。但最新研究揭示,在GLP-1R被激活的背景下,GIPR的共激活不仅能协同增强餐后胰岛素分泌,还可能通过中枢或外周机制,减轻GLP-1R单药引发的胃肠道不良反应,从而提升整体治疗依从性。此外,GIP对脂肪组织功能和骨代谢的潜在调节作用,为多重激动剂带来额外获益。
2.3. GCGR:解锁能量代谢的“关键引擎”
胰高血糖素受体(GCGR)的激活能直接促进肝脏脂质氧化、增加能量消耗、改善线粒体功能,并可能抑制肝星状细胞活化,可直接靶向重度肥胖和肝脏脂肪堆积。然而,单用GCGR激动剂会显著高血糖,限制了其临床应用。通过将其与GLP-1RA结合,可在保留其强效减脂与抗纤维化潜力的同时,由GLP-1R的活性来缓冲其升糖效应,实现“扬长避短”的协同作用。
多靶点协同的本质,是重构一个更接近生理状态的代谢调控网络。GLP-1、GIP和胰高血糖素在体内本就在时序和功能上相互协同与制衡。多重激动剂通过单一分子模拟这一复杂网络的激活状态,从而在胰腺、肝脏、脂肪组织、中枢神经系统等多个器官层面,实现更高效、更生理性的代谢稳态重建。
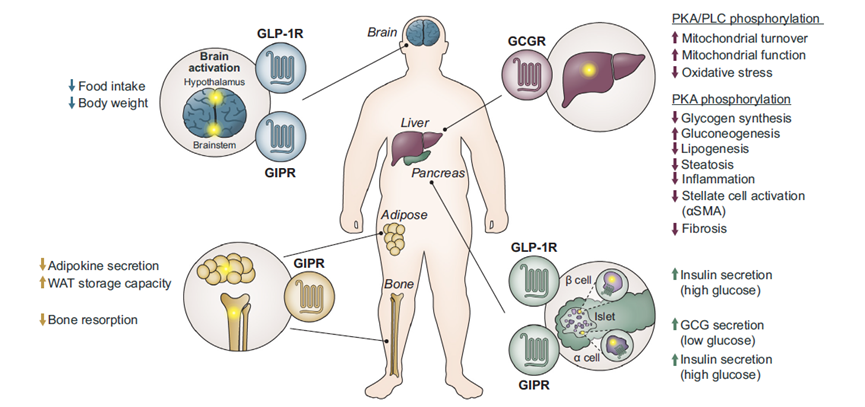
主要肠道激素及其受体激动剂的作用模式和作用部位
10.1016/j.jhep.2023.07.033
这一复杂网络的模拟与验证,对临床前研究平台提出了很高要求。 澎立生物的代谢疾病研究平台,通过建立高度模拟人类病理生理特征的动物模型(如饮食诱导的肥胖模型、NAFLD/MASH模型等),能够系统评估药物对各靶点的激活效应及其协同作用,为多重激动剂的分子设计和机制验证提供关键支撑。
3、临床进展:从概念验证到疗效突破
3.1. 双重激动剂:协同增效的成功验证
以替尔泊肽(GLP-1R/GIPR双重激动剂)为代表的药物已实现从实验室到临床的转化。其SURPASS系列III期临床试验证实,其降糖(如SURPASS-2中HbA1c降低2.3%)与减重(同期减重10.3公斤)疗效显著超越GLP-1R单靶点激动剂(如司美格鲁肽),并展现出明确的心血管安全性。
同时,针对GLP-1R/GCGR组合的双重激动剂(如伊菲诺培肽、科塔度肽)在II期研究中,于降低肝脏脂肪含量和改善非酒精性脂肪性肝炎组织学评分方面展现出独特优势,为代谢性肝病的药物治疗开辟了新路径。
3.2. 三重激动剂:疗效边界的前沿探索
以瑞他鲁肽(GLP-1R/GIPR/GCGR三重激动剂)为代表的三靶点药物,正将代谢改善的效能推向新高度。其发表于《新英格兰医学杂志》的II期研究数据显示,最高剂量组在48周内实现了平均24.2%的体重下降,且疗效呈剂量依赖性,安全性特征与现有药物相似,现已快速进入III期临床。另一款三重激动剂HM15211也在MASH和肥胖领域显示出巨大潜力,为代谢相关疾病治疗提供了新的探索方向。
现有临床数据提示,从单靶点到双靶点、再到三靶点激动剂,疗效呈现阶梯式增强的趋势,且在当前随访周期内,其安全性特征总体可控,未观察到与疗效提升不成比例的风险增加。这标志着多靶点策略在攻克复杂代谢性疾病方面的科学假设,已得到一定程度的验证。
GLP-1RA的跨界潜能与肝脏疾病模型验
如果有一种药物,在高效控制血糖和体重的同时,还能降低心脏病风险、延缓记忆衰退、保护关节、甚至改善脂肪肝,你是否会觉得不可思议?这并非科幻,而是正在成为现实的医学突破。GLP-1RA,这位“代谢管家”,正凭借其遍布全身的作用靶点,逐步展现出作为“健康多面手”的惊人潜能。其中,其在肝脏疾病,尤其是代谢相关脂肪性肝病(MAFLD)/代谢功能障碍相关脂肪性肝炎(MASH)治疗领域的突破,尤为引人注目。
4、一把遍布全身的“万能锁”
GLP-1RA之所以能跨界发挥作用,关键在于其作用靶点——GLP-1受体,在体内分布广泛。这把“锁”不仅存在于胰腺、大脑、心脏和骨骼中,也被报道分布于肝脏相关细胞(如肝星状细胞、免疫细胞等),并可通过直接或间接机制调控肝脏代谢与炎症状态。
因此,当GLP-1RA这把“钥匙”在体内循环时,它能开启包括肝脏在内的多个系统的生理调节功能,传递抗炎、抗氧化应激、抑制纤维化、改善能量代谢等核心信号。这些作用构成了其跨界治疗潜能的基础。
5、肝脏:从“代谢负担”到“治疗前沿”
肝脏是GLP-1RA发挥跨界保护作用的关键器官之一。随着肥胖和代谢综合征的流行,MAFLD/MASH已成为全球最常见的慢性肝病之一,GLP-1RA通过多重机制,为这一难题提供了新的解决思路。
1. 核心作用机制:多通路协同改善肝病
减少肝脏脂肪沉积:通过激活AMPK信号通路,抑制肝脏新生脂肪生成,并促进脂肪酸β-氧化,从源头减少肝细胞内脂质堆积。
抗炎与抗纤维化:通过抑制NF-κB等炎症通路,降低TNF-α、IL-1β等促炎因子表达,减轻肝脏炎症损伤。同时,能抑制肝星状细胞的活化,减少胶原沉积,从而延缓甚至逆转肝纤维化进程。
改善全身代谢:通过减轻体重、改善胰岛素抵抗和调节脂质代谢,间接减轻肝脏的代谢负担。
2. 临床证据与未来方向
临床研究已证实,司美格鲁肽等GLP-1RA能显著降低肝脏脂肪含量、改善肝脏酶学指标(如ALT、AST)。更令人瞩目的是,以GLP-1R/GIPR双靶点激动剂(如替尔泊肽)和GLP-1R/GIPR/GCGR三靶点激动剂(如瑞他鲁肽)为代表的多重激动剂,在临床试验中显示出超越单靶点药物的肝病改善潜力。
研究显示,这类药物不仅能更高效地降低肝脏脂肪含量,还能通过更强的抗炎和代谢调节作用,更显著地改善肝脏炎症和纤维化标志物。例如,GLP-1R/GIPR双靶点激动剂在头对头比较中,其降低肝脏脂肪的效果优于单靶点GLP-1RA,为MASH的治疗提供了更优解。
6、心脏、大脑与骨骼的“跨界守护”
除了肝脏,GLP-1RA在其他系统的保护作用同样令人振奋:
心脏与血管:大型心血管结局试验证实,其能显著降低2型糖尿病患者的主要心血管不良事件风险,已成为兼具心血管获益的降糖基石药物。
大脑:研究表明,GLP-1RA可能通过抗炎、减少异常蛋白沉积等机制,在阿尔茨海默病、帕金森病等神经退行性疾病中发挥积极作用,为这类疾病提供潜在的治疗方向。
骨骼与关节:研究表明,其能通过调节骨代谢、抑制软骨降解和减轻关节炎症,对骨质疏松和骨关节炎产生潜在有益影响。
这些跨领域的益处共同揭示,GLP-1RA的作用远超单纯的代谢调节,它是一种具有系统性抗炎和器官保护潜能的“多效性”治疗剂。
7、未来展望与平台支撑:澎立生物代谢平台
多重激动剂的研究已超越单纯的减重和降糖,进入探索全身多器官保护的新阶段。未来的研究焦点将深入探索其在心血管疾病、阿尔茨海默病等与代谢密切相关的慢性疾病中的长期获益与风险,旨在提供一种“一石多鸟”的系统性健康解决方案。
这一革命性疗法的成功研发,高度依赖于能够精准模拟人类复杂代谢疾病、并有效验证多靶点协同机制的临床前研究平台。 澎立生物凭借其深厚的代谢疾病研究经验,建立了全面且转化相关性强的临床前疾病模型与评价体系。从单纯性肥胖、糖尿病到复杂的MASH及肝纤维化模型,澎立平台能够为包括GLP-1多重激动剂在内的创新代谢药物,提供从机制探索、药效验证到安全性评估的一站式解决方案,为新药研发从“靶点协同”的科学构想,走向“全身获益”的临床现实,提供不可或缺的坚实桥梁。

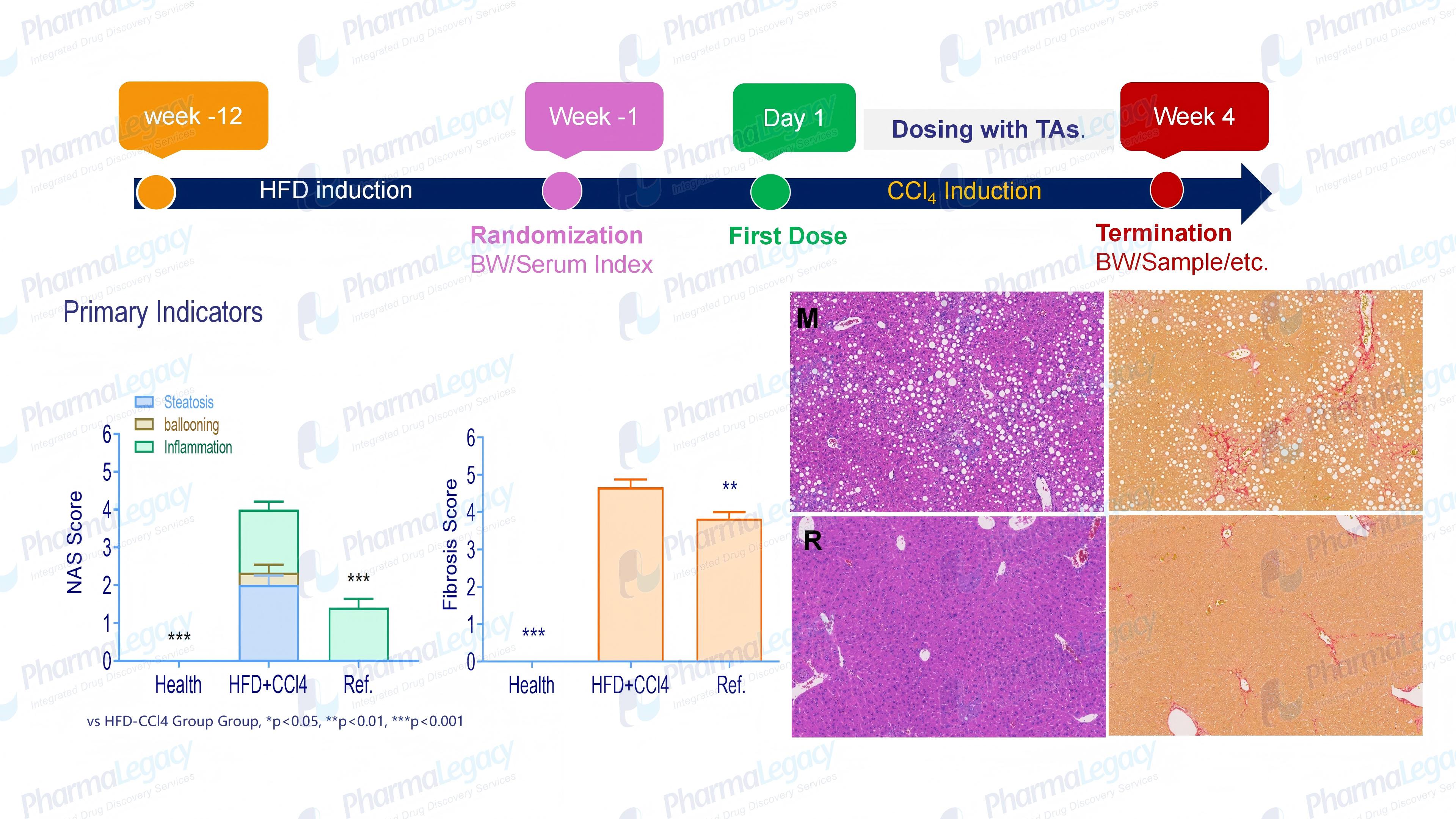
HFD+CCl4诱导的MASH模型案例
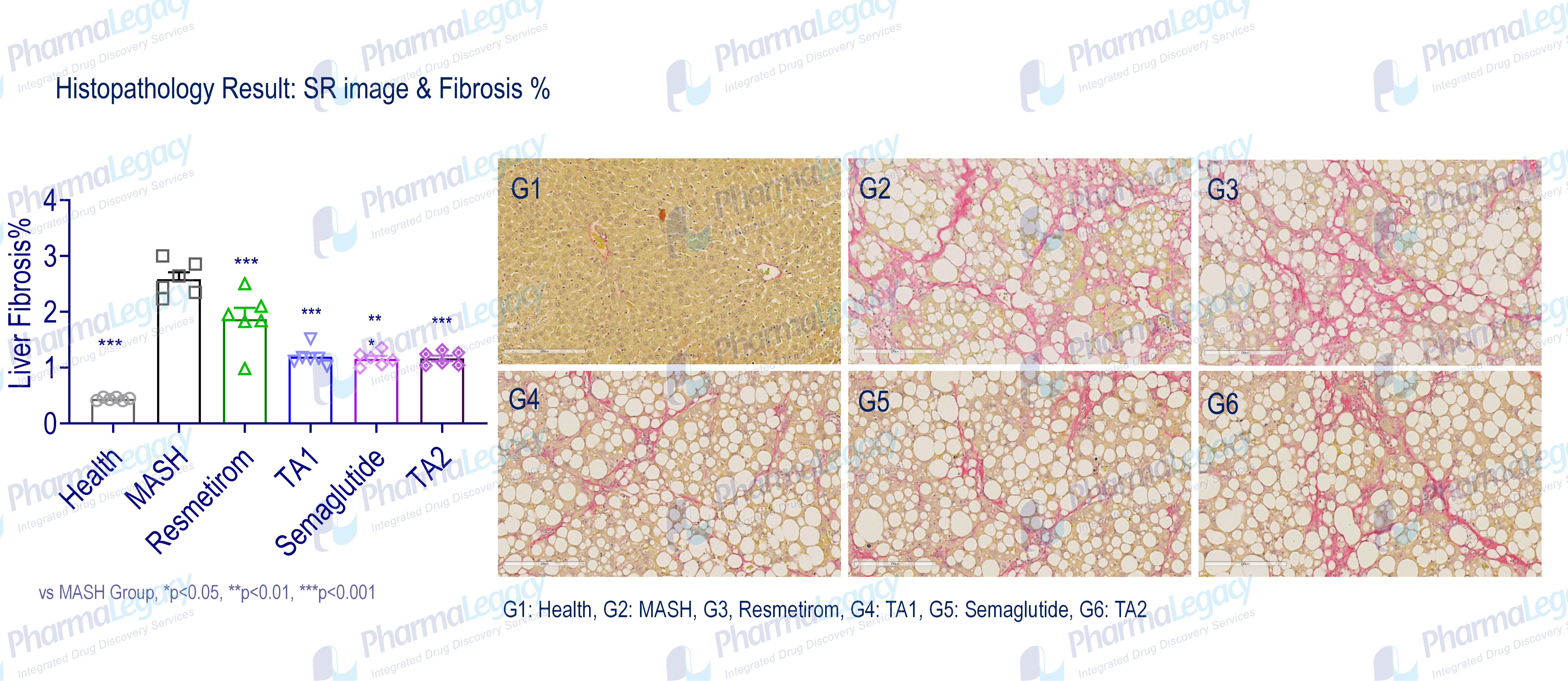
CDAHFD诱导的MASH模型案例
参考文献:
[1] Nauck MA, D'Alessio DA. Tirzepatide, a dual GIP/GLP-1 receptor co-agonist for the treatment of type 2 diabetes with unmatched effectiveness regrading glycaemic control and body weight reduction. Cardiovasc Diabetol. 2022 Sep 1;21(1):169.
[2] Zhao F, Zhou Q, Cong Z, Hang K, Zou X, Zhang C, Chen Y, Dai A, Liang A, Ming Q, Wang M, Chen LN, Xu P, Chang R, Feng W, Xia T, Zhang Y, Wu B, Yang D, Zhao L, Xu HE, Wang MW. Structural insights into multiplexed pharmacological actions of tirzepatide and peptide 20 at the GIP, GLP-1 or glucagon receptors. Nat Commun. 2022 Feb 25;13(1):1057.
[3] Newsome PN, Ambery P. Incretins (GLP-1 receptor agonists and dual/triple agonists) and the liver. J Hepatol. 2023 Dec;79(6):1557-1565.
[4] Rosenstock J, Wysham C, Frías JP, Kaneko S, Lee CJ, Fernández Landó L, Mao H, Cui X, Karanikas CA, Thieu VT. Efficacy and safety of a novel dual GIP and GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1): a double-blind, randomised, phase 3 trial. Lancet. 2021 Jul 10;398(10295):143-155. doi: 10.1016/S0140-6736(21)01324-6. Epub 2021 Jun 27. Erratum in: Lancet. 2021 Jul 17;398(10296):212.
[5] Del Prato S, Kahn SE, Pavo I, Weerakkody GJ, Yang Z, Doupis J, Aizenberg D, Wynne AG, Riesmeyer JS, Heine RJ, Wiese RJ; SURPASS-4 Investigators. Tirzepatide versus insulin glargine in type 2 diabetes and increased cardiovascular risk (SURPASS-4): a randomised, open-label, parallel-group, multicentre, phase 3 trial. Lancet. 2021 Nov 13;398(10313):1811-1824.
[6] Garvey WT, Frias JP, Jastreboff AM, le Roux CW, Sattar N, Aizenberg D, Mao H, Zhang S, Ahmad NN, Bunck MC, Benabbad I, Zhang XM; SURMOUNT-2 investigators. Tirzepatide once weekly for the treatment of obesity in people with type 2 diabetes (SURMOUNT-2): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet. 2023 Aug 19;402(10402):613-626.
[7] Romero-Gómez M, Lawitz E, Shankar RR, Chaudhri E, Liu J, Lam RLH, Kaufman KD, Engel SS; MK-6024 P001 Study Group. A phase IIa active-comparator-controlled study to evaluate the efficacy and safety of efinopegdutide in patients with non-alcoholic fatty liver disease. J Hepatol. 2023 Oct;79(4):888-897.
[8] Nahra R, Wang T, Gadde KM, Oscarsson J, Stumvoll M, Jermutus L, Hirshberg B, Ambery P. Effects of Cotadutide on Metabolic and Hepatic Parameters in Adults With Overweight or Obesity and Type 2 Diabetes: A 54-Week Randomized Phase 2b Study. Diabetes Care. 2021 Jun;44(6):1433-1442. doi: 10.2337/dc20-2151. Epub 2021 May 20. Erratum in: Diabetes Care. 2022 Dec 1;45(12):3112.
[9] Rosenstock J, Frias J, Jastreboff AM, Du Y, Lou J, Gurbuz S, Thomas MK, Hartman ML, Haupt A, Milicevic Z, Coskun T. Retatrutide, a GIP, GLP-1 and glucagon receptor agonist, for people with type 2 diabetes: a randomised, double-blind, placebo and active-controlled, parallel-group, phase 2 trial conducted in the USA. Lancet. 2023 Aug 12;402(10401):529-544.
[10] Zheng Z, Zong Y, Ma Y, Tian Y, Pang Y, Zhang C, Gao J. Glucagon-like peptide-1 receptor: mechanisms and advances in therapy. Signal Transduct Target Ther. 2024 Sep 18;9(1):234.
[11] Jastreboff AM, Kaplan LM, Frías JP, Wu Q, Du Y, Gurbuz S, Coskun T, Haupt A, Milicevic Z, Hartman ML; Retatrutide Phase 2 Obesity Trial Investigators. Triple-Hormone-Receptor Agonist Retatrutide for Obesity - A Phase 2 Trial. N Engl J Med. 2023 Aug 10;389(6):514-526.
[12] Fernandez Rico C, Konate K, Josse E, Nargeot J, Barrère-Lemaire S, Boisguérin P. Therapeutic Peptides to Treat Myocardial Ischemia-Reperfusion Injury. Front Cardiovasc Med. 2022 Feb 17;9:792885.
[13] Wang D, Luo P, Wang Y, Li W, Wang C, Sun D, Zhang R, Su T, Ma X, Zeng C, Wang H, Ren J, Cao F. Glucagon-like peptide-1 protects against cardiac microvascular injury in diabetes via a cAMP/PKA/Rho-dependent mechanism. Diabetes. 2013 May;62(5):1697-708.
[14] Marso SP, Bain SC, Consoli A, Eliaschewitz FG, Jódar E, Leiter LA, Lingvay I, Rosenstock J, Seufert J, Warren ML, Woo V, Hansen O, Holst AG, Pettersson J, Vilsbøll T; SUSTAIN-6 Investigators. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med. 2016 Nov 10;375(19):1834-1844.
[15] Cai HY, Yang JT, Wang ZJ, Zhang J, Yang W, Wu MN, Qi JS. Lixisenatide reduces amyloid plaques, neurofibrillary tangles and neuroinflammation in an APP/PS1/tau mouse model of Alzheimer's disease. Biochem Biophys Res Commun. 2018 Jan 1;495(1):1034-1040.